Publié le 15 mar 2010Lecture 10 min
Traitement de l’asthme de l'enfant : vers un meilleur contrôle
J. dE BLIC, Hôpital Necker – Enfants Malades, Paris
La prise en charge de l’enfant asthmatique a connu ces dernières années plus d’évolution que de révolution. La vraie révolution avait eu lieu dans les années 80, lorsque d’une pathologie essentiellement du muscle lisse bronchique, l’asthme est devenu une maladie inflammatoire avec comme corollaire le passage d’un traitement basé uniquement sur les bronchodilatateurs à un traitement de fond par les corticoïdes inhalés.
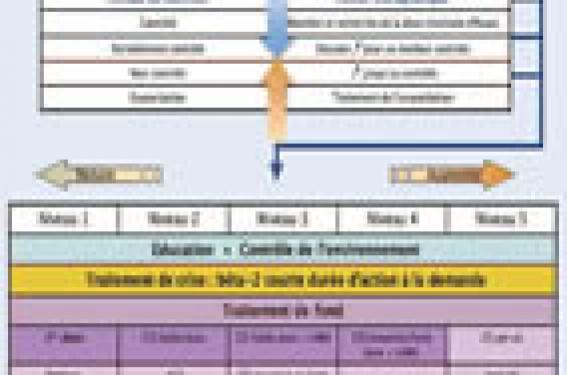
Maladie chronique parmi les plus fréquentes chez l’enfant, l’asthme a une prévalence de 8 à 10 %. Après des années d’augmentation constante, cette prévalence reste stable. En France, la mortalité par asthme a bien heureusement diminué au cours de ces dernières années. En 2005, le taux de mortalité chez les moins de 15 ans était de 0,1 pour 100 000 habitants chez les garçons et chez les filles, soit 8 décès dont 3 chez des enfants de 1 à 4 ans et 5 chez des enfants de 10 à 14 ans. Le nombre annuel d’hospitalisations reste cependant important et n’a pas diminué surtout chez les moins de 4 ans. Enfin, toutes les enquêtes montrent que les enfants asthmatiques restent trop souvent symptomatiques. Dans une étude récente menée auprès de pédiatres et de généralistes et portant sur plus de 3 000 enfants, plus d’un tiers d’entre eux avaient eu un recours aux soins (consultation de leur médecin en urgence, consultation aux urgences ou hospitalisation) et près de 40 % avaient manqué l’école dans les 6 derniers mois du fait de symptômes d’asthme. De la notion de sévérité à celle du contrôle L’objectif de la prise en charge de l’enfant asthmatique est double, permettre à l’enfant de mener une vie normale avec des fonctions pulmonaires normales. Mener une vie normale signifie un minimum de symptômes le jour comme la nuit, au repos comme à l’effort, avec une consommation minimale de bronchodilatateurs de secours et des traitements bien tolérés. Des recommandations trop rigides inapplicables Les recommandations internationales ont été basées sur le degré de sévérité de l’asthme des patients, adultes comme enfants. On distinguait ainsi 4 stades : les asthmes intermittents et les asthmes persistants léger, modéré et sévère selon la fréquence des symptômes diurnes et nocturnes, la fréquence et la sévérité des exacerbations, le VEMS et les variations nycthémérales du débit de pointe. À chaque stade était affecté un schéma thérapeutique : pas de traitement de fond pour les asthmes intermittents ; corticoïdes inhalés (CSI) faible dose en cas d’asthme persistant léger ; association de CSI et β2-agonistes de longue action (β2LA) dans les formes modérées et sévères. Ce type de recommandations avait malheureusement beaucoup d’inconvénients. Les critères adultes et pédiatriques étaient les mêmes alors que les objectifs sont probablement plus ambitieux chez l’enfant que chez l’adulte, aussi bien sur le plan des symptômes que de la fonction respiratoire. Par ailleurs, les critères n’étaient pas les mêmes selon les recommandations internationales et/ou nationales. Surtout, ces recommandations figeaient le patient dans un niveau de sévérité et donc dans un schéma thérapeutique rigide. Elles ne prenaient pas en compte la variabilité temporelle des symptômes et avaient des seuils de fonction respiratoire (DEP et VEMS) inadaptés chez l’enfant, car restant le plus souvent dans les limites de la normale, y compris pour les asthmes sévères. D’autre part, un biais pouvait être induit par un éventuel traitement de fond déjà institué, En fin de compte, trop compliquées et variables ces recommandations n’étaient ni applicables ni appliquées. Recommandations et notion de contrôle Les recommandations insistent désormais sur la notion de contrôle qui traduit la maîtrise de l’asthme et reflète donc l’activité, le caractère dynamique de la maladie sur quelques semaines. Cette notion est valable quelle que soit la sévérité de l’asthme. Des critères de contrôle ont été proposés par le Global INititiative for Asthma (GINA) et le National Institutes of Health (NIH) par l’intermédiaire du National Asthma Education and Prevention Program. Le contrôle total, défini par l’absence de symptômes et par une fonction respiratoire normale, doit être l’objectif chez l’enfant. S’il existe encore quelques différences dans les items retenus et l’intervalle étudié, ces recommandations ont l’avantage d’insister sur le caractère modulable du traitement (figure). Cette dernière notion implique un suivi régulier allant d’une fois par an pour ceux dont la pression thérapeutique est la plus faible à une fois par trimestre pour ceux ayant des doses de CSI les plus élevées. Des questionnaires de contrôle peuvent aider à poser les bonnes questions, mais ils ne doivent pas faire omettre la réalisation d’explorations fonctionnelles respiratoires (EFR). Comme cela a été dit plus haut, l’objectif ambitieux est la normalité ou la normalisation des fonctions respiratoires. Elles seules peuvent détecter une obstruction infraclinique non ressentie par l’enfant. Malheureusement, là encore, moins de 20 % des enfants asthmatiques ont eu une EFR et encore moins un suivi d’EFR. Les recommandations actuelles insistent sur la notion de contrôle et sur le caractère modulable du traitement. Les choix thérapeutiques Un traitement classique bien installé Les nouvelles classes thérapeutiques anti-asthmatiques sont rares. La pierre angulaire reste et restera pour encore des années la corticothérapie inhalée. Ce sont des évolutions qui ont permis de mettre à disposition des molécules à effet anti-inflammatoire plus puissant, des bronchodilatateurs dont l’action était plus prolongée (les β2LA), des galéniques et des dispositifs d’inhalation plus adaptés à l’enfant (poudre sèche), des molécules actives par voie orale (les antileucotriènes). C’est toujours le souci de la dose minimale efficace qui doit être présent à l’esprit, surtout en matière de corticoïdes inhalés. Si les doses standards sont bien tolérées en termes de croissance, de déminéralisation, de retentissement sur l’axe hypothalamo-hypophysaire, il existe un effet systémique dose-dépendant (et des décès par insuffisance surrénale aigus comme des syndromes de Cushing ont été décrits) et on ne connaît pas aujourd’hui le retentissement sur la minéralisation à très long terme, par exemple après 40 ans de CSI… Le souci de la dose minimale efficace doit toujours être présent à l’esprit, surtout en matière de corticoïdes inhalés. Les nouvelles thérapies ciblées : pour les asthmes sévères Le bon usage de ces traitements permet théoriquement d’obtenir le contrôle chez plus de 95 % des enfants asthmatiques. Les évolutions thérapeutiques viendront essentiellement de nouvelles galéniques ou de nouvelles molécules, qui permettront par exemple de limiter encore les prises de bronchodilatateur longue durée à une par jour. Les réelles nouvelles classes thérapeutiques ne concerneront que la faible proportion d’asthme qualifié de sévère, difficile, rebelle ou intraitable. On s’approchera alors plus d’une thérapeutique ciblée sur une ou plusieurs molécules impliquées dans la physiopathologie de l’asthme. Les anticorps anti-IgE ouvrent la voie à ces nouvelles thérapeutiques ciblées. L’omalizumab est un anticorps monoclonal humanisé d’origine murine qui se lie aux IgE circulantes, empêchant leur fixation sur leurs récepteurs cellulaires. Il s’administre par voie sous-cutanée toutes les 2 à 4 semaines à une posologie dépendante du poids et du taux initial d’IgE. Sa tolérance semble bonne chez l’enfant. L’efficacité est optimale quand l’asthme est sévère, avec une réduction du taux d’exacerbations, une réduction du recours aux traitements d’urgence et une amélioration de la qualité de vie. Peut-on modifier l’histoire naturelle de l’asthme ? Les études historiques de cohortes telles que la cohorte de Melbourne qui a suivi des asthmatiques de 7 à 42 ans, mais surtout les analyses prospectives de cohortes pédiatriques (cohorte de Tucson dans l’Arizona, cohorte MAS [Multicenter Allergic Study] en Allemagne, ou encore cohorte de Manchester en Angleterre) ont permis de mieux connaître l’histoire naturelle de l’asthme et de l’allergie. Les deux points importants sont, d’une part, la notion de tracking ou de couloir clinique et fonctionnel et, d’autre part, le rôle important voire prépondérant du terrain atopique. ● Le tracking. La notion de couloir fait référence au fait que les symptômes comme le degré d’obstruction bronchique restent stables tout au long de l’enfance. En d’autres termes, les asthmatiques sévères resteront sévères : l’obstruction bronchique apparaît tôt dans la vie et persiste. De même, les anomalies de remodelage bronchique qui traduisent la réponse aux phénomènes inflammatoires associés à l’asthme peuvent apparaître très tôt dans la vie. ● Le poids de l’atopie. Le deuxième point important des analyses de cohortes est le poids très important de l’atopie, aussi bien dans la persistance des symptômes du nourrisson à l’enfant puis à l’adulte que dans la sévérité clinique ou fonctionnelle. Plusieurs essais ont été réalisés pour tester l’hypothèse qu’une corticothérapie inhalée précoce était susceptible de modifier l’histoire naturelle du nourrisson. Les résultats se sont révélés décevants, démontrant le caractère uniquement suspensif des CSI, avec un retour à l’état antérieur dès leur arrêt. Il ne faut pas pour autant tirer des conclusions négatives définitives. Dans la PEAK study (Prevention of Early Asthma in Kids) où les auteurs ont évalué les CSI en double aveugle versus placebo, les CSI avaient été introduits en moyenne à l’âge de 3 ans et près de 18 mois après le début des manifestations, donc probablement trop tard pour modifier l’histoire naturelle de l’asthme. Le terrain atopique pèse doublement sur la symptomatologie et la sévérité de l’asthme. ● En fait, la solution viendra peutêtre de la désensibilisation spécifique. Une étude pilote a montré que la désensibilisation aux pollens de graminées ou de bouleau chez des enfants ayant une rhinite allergique saisonnière permettait, par rapport au groupe placebo, une diminution significative du risque d’apparition d’asthme et que cet effet persistait plus de 5 ans après l’arrêt de la désensibilisation. Une autre étude a montré que chez de jeunes enfants, la désensibilisation aux acariens diminuait significativement l’apparition d’autres sensibilisations. Plus qu’un simple traitement symptomatique, la dé-sensibilisation spécifique pourrait donc modifier l’histoire naturelle de l’asthme. Le poids de l’allergie dans l’asthme et le caractère plus « pur » et moins polyfactoriel (pollution, tabagisme, milieu professionnel, vieillissement) chez l’enfant par rapport à l’adulte méritent les études prospectives à venir. Conclusion En définitive, la prise en charge de l’asthme de l’enfant est à la fois simple et complexe. Simple parce que les classes thérapeutiques sont peu nombreuses mais efficaces pour l’immense majorité des enfants. Complexe parce que l’asthme est multifactoriel dans ses facteurs déclenchants en particulier. Paradoxalement, c’est encore une maladie qui souffre d’un retard diagnostique et donc d’un retard et d’une insuffisance de traitement. Beaucoup de travail et d’éducation thérapeutique restent encore à faire.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :