Publié le 24 mar 2025Lecture 8 min
Dermatologie pédiatrique : apport des données récentes de la littérature
Catherine FABER, d’après la communication de Stéphanie Mallet (hôpital de la Timone, Marseille)

Les données présentées lors de la traditionnelle session « Quoi de neuf » des Journées dermatologiques de Paris (JDP) témoignent de la richesse de l’actualité dans ce champ de la pédiatrie.
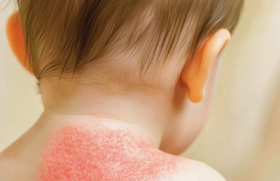
Dermatite atopique et autres dermatoses inflammatoires
Les enfants atteints de dermatite atopique (DA) présentent un risque accru de développer des infections. Leur risque infectieux est-il favorisé par les biothérapies ? La réponse à cette question légitime est apportée par l’analyse des données de l’essai randomisé de phase 3 du dupilumab chez les enfants de 6 mois à 5 ans (LIBERTY AD PRESCHOOL)(1). Ce travail montre que le dupilumab n’augmente pas le risque global d’infection. Au contraire, il diminue le risque d’infections cutanées bactériennes et d’infections cutanées non herpétiques, ainsi que la consommation d’anti-infectieux. D’autres données récentes concernant l’utilisation concomitante de vaccins vivants et vivants atténués avec le dupilumab sont également rassurantes. Dans le même essai pédiatrique, aucun effet indésirable n’a été constaté chez les 9 enfants qui avaient reçu un vaccin ROR ou l’association RORvaccin antivaricelle(2). Il faut toutefois rester prudent et continuer à se con former aux recommandations indiquant que le traitement immunosuppresseur, la corticothérapie et/ou les biothérapies doivent être arrêtées 3 mois avant d’administrer ce type de vaccin, puis repris après 4 semaines (ROR, vaccin fièvre jaune) ou 6 semaines (vaccin VZV).
Une petite série de cas (4 patients de 2 à 8 ans) suggère l’intérêt potentiel du dupilumab dans la réaction du greffon contre l’hôte (GVH) eczématiforme, résistante aux traitements immuno-suppresseurs(3). Il a entraîné une amélioration de la GVH dans les 12 semaines et permis un sevrage rapide des immunosuppresseurs. Dans la GVH sclérodermiforme réfractaire aussi, une amélioration sous dupilumab a été observée dans deux cas d’enfants rapportés(4). Ces résultats devront être confirmés.
Deux publications récentes sont consacrées aux traitements systémiques conventionnels dans la prise en charge de la DA et d’autres dermatoses inflammatoires chroniques. L’essai randomisé comparatif TREAT, mené chez 103 enfants avec DA sévère, a montré que la ciclosporine et le méthotrexate (MTX) sont tous deux efficaces(5). La ciclosporine (AMM chez les plus de 16 ans) agit plus rapidement, mais le MTX (hors AMM) permet un contrôle plus durable, même après arrêt du traitement. Des recommandations sur le traitement par MTX dans les dermatoses inflammatoires pédiatriques ont été établis par un collectif d’experts américains(6). Le système d’aide à la prescription proposé rappelle que la posologie maximale est de 1 mg/kg/semaine (maximum 25 mg/semaine), que la dose test n’est pas nécessaire et que l’association avec les AINS et les rappels de vaccins vivants (ROR et VZV) ne sont pas contre-indiqués. Les experts précisent qu’en l’absence de données suffisantes, la primovaccination avec le ROR n’est pas autorisée.
Dans la pelade, l’actualité est faite par l’essai de phase 2 b/3 du double inhibiteur oral de JAK3/TEC ritlécitinib (ALLEGRO)(7). Il a inclus 105 adolescents de 12 à 17 ans atteints de pelade sévère (perte de cheveux > 50 %). À la semaine 24, une proportion significativement plus importante de patients a eu une repousse des cheveux avec le ritlécitinib 50 mg ou 30 mg/j versus la dose de 10 mg ou le placebo. La re pousse s’est poursuivie et, à la semaine 48, 50 % des patients sous ritlécitinib 50 mg avaient une repousse couvrant plus de 80 % de leur cuir chevelu. Le ritlécitinib est le premier médicament à obtenir une AMM dans le traitement de la pelade sévère à partir de l’âge de 12 ans. Il s’agit d’un traitement suspensif, remboursé à 30 %.
Les anomalies vasculaires
L’évolution à long terme (≥ 10 ans) du syndrome PHACE (Posterior fossa anomalies, Hemangiomas, Arterial anomalie, Cardiac abnormalities and coarctation of aorta, Eye anomalies) est désormais connu grâce à une étude sur 104 patients d’âge médian de 14 ans (10-77 ans)(8). Plus de neuf patients sur 10 (94 %) présentaient des séquelles cutanées principalement à type de couleur, de texture et de volume (respectivement 71 %, 39 % et 22 %). La moitié avait reçu un traitement de l’hémangiome infantile résiduel par laser vasculaire et 89,5 % étaient satisfaits ou très satisfaits. En revanche, leur devenir neurologique est moins bon. Près des trois quarts des patients (72 %) avaient des maux de tête/des migraines, 45 % des difficultés d’apprentissage et 39 % avaient eu recours à un plan d’enseignement individualisé. L’étude montre une prévalence élevée de l’artériopathie cérébrale (91 %). Dans près d’un tiers des cas (29 %), elle était évolutive, mais moins de 2 % des patients avaient fait un accident vasculaire cérébrale ischémique. Compte tenu de cette morbidité à long terme parfois sévère du syndrome, un suivi au long cours des patients doit être instauré.
Les syndromes hypertrophiques avec malformations vasculaires cutanées sont classiquement dus à une mutation du gène PIK3CA. D’où la désignation de syndrome PROS pour « syndrome hypertrophique lié à PIK3CA » (PIK3CA-Related Overgrowth Spectrum). Une équipe française a constaté dans une cohorte de 213 patients négatifs pour la mutation classique que 7 % étaient positifs pour PIK3R1, avec un phénotype de syndrome de Klippel-Trenaunay(9). Elle propose de modifier la signification de l’acronyme PROS en « spectre de prolifération lié à PI3K » (PI3KRelated Overgrowth Spectrum) pour inclure à la fois les phénotypes liés à PIK3CA et PIK3R1. L’étude multicentrique rétrospective EPIK-P1 (n = 39 enfants de plus de 2 ans et 18 adultes) suggère que l’alpélisib, un inhibiteur sélectif de PI3Ka, est efficace dans le traitement du syndrome PROS(10). Il a permis de réduire les lésions cibles à l’IRM chez 74 % des patients, d’au moins 20 % du volume chez 37,4 % d’entre eux. L’amélioration clinique est rapide, dès la 12e semaine de traitement, mais modeste. Des effets secondaires sont apparus dans 38,6 % des cas, notamment une hyperglycémie qui devra être dépistée chez les patients. L’alpélisib est actuellement disponible en accès précoce. Un essai randomisé prospectif de phase 2 est en cours (EPIK-P2).
Enfin, deux grandes études publiées en 2024 portaient sur le syndrome BASCULE (Bier Anaemic Spots and Cyanosis with Urticarial-Like Eruption). Cette dermatose vasomotrice « bleu, blanc, rouge », se manifeste par l’apparition successive d’une acrocyanose (bleu), de macules anémiques (blanc) et d’une éruption pseudo-urticarienne (rouge). Les études ont inclus 17 et 42 patients d’âge médian de 12 ans(11,12). Elles mettent en évidence l’atteinte élective des membres et montrent que le syndrome survient en position orthostatique et est déclenché principalement par des douches chaudes. Près de 60 % des patients avaient un dysfonctionnement du système nerveux autonome de type tachycardie orthostatique posturale (respectivement 24 % et 12,5 % dans les deux études) ou une intolérance orthostatique chronique (18 % et 59 %). Dans la seconde étude, 47 % des ado lescents avaient un TDAH, 41 % prenaient des psychostimulants et 29 % avaient souffert de Covid-19. La prise de psychostimulants dans le cadre d’un TDAH pourrait favoriser la dysautonomie et ferait le lit du syndrome BASCULE.
Les génodermatoses
La littérature récente fait état d’une innovation thérapeutique dans l’épidermolyse bulleuse dystrophique et d’un possible repositionnement des biologiques et des inhibiteurs de JAK (iJAK) dans les ichtyoses. Une équipe américaine a réalisé la première thérapie topique chez un adolescent de 13 ans atteint d’épidermolyse bulleuse dystrophique (B-VEC en collyre après chirurgie)(13). Une cicatrisation complète de la cornée, mais également une amélioration de l’acuité visuelle ont été obtenues. Cette observation soulève un grand espoir.
Dans une série rétrospective multicentrique internationale de 98 patients de 0,6 à 69 ans avec ichtyose congénitale et traités pendant plus de 3 mois avec un biologique, 46 % étaient répondeurs, dont 18 % bons répondeurs(14). Les résultats sont décevants car l’efficacité est modérée et surtout transitoire. L’étude a néanmoins montré que les formes répondant le mieux étaient, logiquement, les formes inflammatoires (syndrome de Netherton et érythrodermie congénitale ichtyosiforme). Les anti-IL12/23 ou les anti-IL4/13 se sont révélés plus efficaces que les anti-IL17. Dans le syndrome de Netherton, il a été montré que l’upadacitinib, un inhibiteur de JAK, entraîne une amélioration modérée et transitoire d’abord chez l’adulte et, pour la première fois en 2024, également chez l’adolescent (1 cas rapporté chez un enfant de 14 ans)(15).
Les nævus
Les nævus congénitaux sont associés à des mutations en mosaïque, essentiellement du gène NRAS (65 %). Dans 25 % des cas, la mutation est inconnue. Les auteurs d’une étude sur 169 patients sans cause génétique identifiée ont mis en évidence des mutations du gène de BRAF en mosaïque et de fusion RAF1 chez respectivement 11 et 1 patient(16). On a donc un diagnostic génétique pour un groupe supplémentaire de patients avec une option thérapeutique, le trametinib, pour les phénotypes les plus sévères. Cet anti-MK inhibe l’hyperactivation de la voie MAP kinase in vitro et a amélioré rapidement l’hypertrophie et le prurit chez deux patients. Le trametinib a des effets secondaires bien connus, ophtalmologiques, cardiaques et surtout dermatologiques. Une forme topique pourrait avoir les avantages de la molécule sans ses inconvénients. Le trametinib crème 1 % a été utilisé avec succès chez une enfant atteinte d’un syndrome de Schimmelpenning-FeuersteinMims avec un hamartome épidermique muté KRAS réfractaire au tazarotène et au 5FU(17). L’évaluation du traitement montre une amélioration avec un amincissement des lésions et une diminution du prurit, avec une parfaite tolérance.
Les dermatoses affichantes
Deux publications se sont intéressées au retentissement des dermatoses chroniques sur la vie quotidienne des patients pédiatriques. Une étude menée sur 1 671 patients âgés de 8 à 17 ans montre que 73 % ressentent une stigmatisation (surtout les jeunes filles), modérée à sévère dans 44 % des cas(18). La stigmatisation ressentie est associée à la visibilité et à la sévérité de la maladie, mais pas toujours. Par conséquent, ces critères sont insuffisants pour évaluer l’impact de la dermatose sur le patient. Il existe aussi une corrélation forte entre le sentiment d’être stigmatisé et le harcèlement, la réduction de la qualité de vie, l’anxiété, la dépression et les relations sociales faibles. La seconde publication émane d’un groupe de travail de l’EADV (European Academy of Dermatology and Venereology) qui a analysé la prévalence et la nature du harcèlement chez 1 016 patients avec 36 dermatoses différentes(19). Un quart d’entre eux (26 %) indique avoir été harcelé en consultation et 64 % via les réseaux sociaux. Les 13-15 ans sont les plus touchés, mais le harcèlement peut commencer dès l’âge de 3 ans. Il faut donc être vigilant dès le plus jeune âge. Les formes de harcèlement les plus fréquentes sont les abus verbaux et l’isolement social. Seules 33 % des victimes en ont parlé et 63 % disent avoir des conséquences à long terme du harcèlement. Ces données montrent la nécessité de dépister le harcèlement et d’accompagner les patients qui en sont victimes.
D’après la communication de Stéphanie Mallet (hôpital de la Timone, Marseille) lors de la session « Quoi de neuf » des JDP 2024
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :