Publié le 14 oct 2010Lecture 6 min
Douleurs tibiales à 13 ans
G. AYOUB, J.-D. LAREDO, Hôpital Lariboisière, Paris
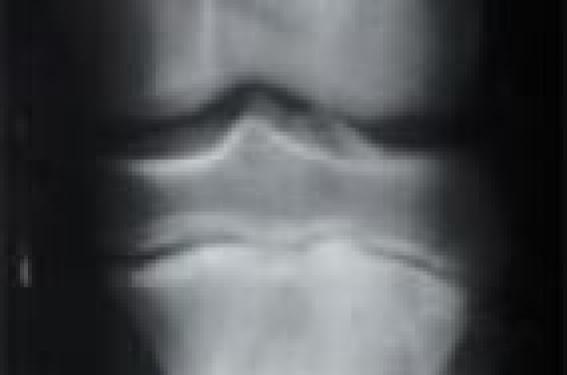
Un adolescent de 13 ans est amené à consulter pour des douleurs tibiales antérieures gauches isolées, qui évoluent depuis plusieurs semaines. Leur apparition n’est rattachée à aucun événement, notamment d’ordre traumatique. L’adolescent n’a d’ailleurs aucun antécédent médical notable. Son examen clinique révèle la présence d’une masse de la face antérieure de l’extrémité supérieure du tibia gauche, sans autre anomalie associée.
Le bilan d’imagerie (radiographie standard et tomodensitométrie) met en évidence une lésion développée au contact de la face antérieure du tibia gauche, de localisation métaphysaire, indépendante du point d’ossification secondaire, qui est le siège de calcifications compatibles avec une matrice cartilagineuse. On note également la présence d’un élargissement métaphysaire, et d’érosions de la corticale sous-jacente, avec ostéosclérose au contact. On remarque, par ailleurs, la présence d’une coque périphérique périostée et l’absence de communication avec le spongieux métaphysaire (figures 1 à 8). Figure 1. Radiographie standard de face du genou gauche montrant une condensation hétérogène et un élargissement de la métaphyse supérieure du tibia. Figure 2. Radiographie standard de profil montrant la lésion ossifiée avec érosion de la face superficielle de la corticale. La lésion se développe à partir du point d’ossification de la tubérosité tibiale antérieure. Figure 3. Radiographie standard du genou gauche, agrandissement sur les calcifications et sur la corticale antérieure, siège d’érosions et d’ostéosclérose. Figure 4. Radiographie standard du genou gauche, avec agrandissement sur les calcifications. Figure 5. Coupe scannographique sagittale montrant les calcifications et la coque fibreuse périostée périphérique. Figure 6. Coupe scannographique axiale montrant les calcifications et la coque fibreuse périostée. Figure 7. Coupe scannographique axiale montrant les rapports entre les calcifications lésionnelles et la face antérieure du tibia, ainsi que l’absence de communication avec le spongieux métaphysaire. Figure 8. Coupe scannographique axiale montrant les érosions de la corticale et la séparation entre le tibia et la lésion calcifiée. Quel est votre diagnostic ? L’ensemble de ces données a permis de conclure au diagnostic de chondrome périosté. Commentaires Le chondrome périosté ou juxtacortical fait partie des tumeurs bénignes cartilagineuses. La forme périostée, qui représente 15 à 20 % des chondromes solitaires, se développe entre la corticale osseuse et le périoste. Cette prolifération de cartilage hyalin à partir du tissu conjonctif paraostéal rend compte de la survenue plus fréquente aux sites d’insertions ligamentaires et tendineuses. Moins de 200 cas de chondrome périosté ont déjà été décrits dans la littérature. Le terrain est marqué par une discrète prédominance masculine, et une survenue entre la 2e et la 3e décennie. Cliniquement, la tumeur peut rester longtemps asymptomatique. Sa découverte se fait donc souvent fortuitement, sur un bilan radiologique demandé pour une autre pathologie. Elle peut se manifester par une douleur locale et un gonflement, corroboré par une masse palpable à l’examen. La localisation élective est à la métaphyse des os longs. Les os les plus fréquemment touchés sont l’humérus proximal dans plus de 25 % des cas, les phalanges dans 17 %, le fémur distal dans près de 10 %, le tibia proximal et le fémur proximal dans 7 %. La taille de la tumeur se situe généralement entre 1 et 3 cm, pouvant poser alors le diagnostic différentiel d’un chondrosarcome. Rarement, la taille dépasse les 5 cm. Macroscopiquement, on retrouve une masse lobulée bleutée, alors que la microscopie met en évidence des lobules de cartilage hyalin, avec des chondrocytes bien différenciés, sans atypie. L’histologie s’attache à éliminer le difficile diagnostic différentiel de chondrosarcome, et recherche toute atypie en sa faveur : hypercellularité, cellules multinucléées, gros noyaux, transformation myxoïde de la matrice, etc. L’interprétation est d’autant plus difficile que ces atypies peuvent également être présentes dans le cadre d’un chondrome périosté. Ainsi, dans une série publiée en 1985, sur 46 chondromes périostés, 72 % présentaient quelques atypies histologiques. La radiographie standard et la tomodensitométrie mettent en évidence une masse tissulaire apposée à la surface de l’os, bien limitée sous le périoste, souvent associée à une érosion de la corticale sous-jacente, avec un aspect en soucoupe. On peut également retrouver une ostéosclérose corticale, qui sépare le chondrome du spongieux métaphysaire, et permet de le distinguer d’une exostose ostéogénique, ainsi que des appositions périostées responsables de fines calcifications périphériques, avec des calcifications cartilagineuses dans près de 50 % des cas. La réaction périostée à la périphérie de la lésion a souvent l’aspect d’un triangle, connu sous le nom de triangle de Codman par les auteurs anglo-saxons. À noter l’absence de communication avec le spongieux métaphysaire. L’IRM, quant à elle, permet l’identification de la matrice cartilagineuse ainsi que l’évaluation de l’extension lésionnelle aux parties molles. Une étude IRM sur 12 cas de chondromes périostés a retrouvé une forme lobulée dans 75 % des cas, avec un signal cartilagineux, hypo- ou iso-intense en T1, et hyperintense en T2 dans 100 % des cas. Tous les cas étaient associés à des érosions corticales, et l’IRM mettait en évidence un plan (fibreux ou osseux) superficiel en hyposignal dans 100 % des cas, contre 25 % seulement sur les radiographies standards. La prise de contraste, essentiellement périphérique, était constante, et des calcifications étaient retrouvées dans la moitié des cas. Le diagnostic différentiel d’un chondrome périosté se pose essentiellement avec les lésions tumorales de surface, qu’elles soient ostéoformatrices (ostéome, ostéome ostéoïde, ostéoblastome, ostéosarcome), cartilagineuses (ostéochondrome, chondrosarcome périosté et paraostéal, fibrome chondromyxoïde périosté), fibreuses (cortical defect, fibrome non ossifiant), graisseuses (lipome paraostéal), vasculaires (hémangiome périosté), ou rarement métastatiques. Les critères radiologiques en faveur de la malignité sont la taille de la tumeur, l’irrégularité de ses limites, une extension intra-médullaire, un oedème intra-médullaire et, surtout, une masse tissulaire développée dans les parties molles ainsi qu’une prise de contraste très précoce, au temps artériel sur les séquences IRM dynamiques après injection de gadolinium. L’évolution du chondrome périosté est généralement bonne, et il n’y a pas de transformation maligne décrite. Le traitement repose sur une résection chirurgicale, avec un taux de récidive de l’ordre de 3,6 %. L’abstention thérapeutique, assortie d’une surveillance régulière, est possible dans les formes asymptomatiques, dont la taille est faible et reste stable dans le temps. Ce qu’il faut retenir sur le chondrome périosté Tumeur cartilagéneuse bénigne. Bon pronostic. Imagerie caractéristique… … Mais diagnostic différentiel difficile en imagerie et en histologie avec le chondrosarcome périosté. Taille lésionnelle importante pour le diagnostic différentiel.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :