Publié le 21 oct 2021Lecture 13 min
Les enfants multiallergiques – Revue critique et conduite à tenir
Guy DUTAU, Allergologue, pneumologue, pédiatre, CHU de Toulouse

Le syndrome des allergies multiples (SAM) se caractérise par la succession et l’association des principales manifestations de l’allergie IgE-dépendante. L’allergie alimentaire (AA) et la dermatite atopique (DA) représentent les premiers symptômes du SAM chez le jeune nourrisson. Ces symptômes évoluent souvent vers des sensibilisations aux pneumallergènes et des allergies respiratoires à type de rhinite et/ou d’asthme. Il est capital de distinguer « sensibilisation » et « allergie ».
Le mot « sensibilisation » est un terme biologique désignant « l’état d’un individu qui possède des IgE spécifiques » que l’on peut détecter par la positivité des prick-tests (PT) et/ou par la présence d’IgE sériques spécifiques (IgEs) mesurés par des dosages biologiques (Rast ou Radio-allergo-sorbent-test et méthodes dérivées). Le mot « allergie » est un terme clinique qui désigne « une réaction anormale, excessive, de l’organisme à un antigène (allergène) auquel il est particulièrement sensible ».
Plus précisément, « sensibilisation » désigne une situation biologique (avec ou sans symptôme clinique) et « allergie » un « événement clinique » (rhinite, asthme, urticaire, troubles digestifs, etc.) pour lequel le patient va consulter. Cette distinction est importante pour la bonne compréhension des symptômes allergiques et le terme de « sensibilisation allergique » est presque un pléonasme, le vocable « sensibilisation IgE-dépendante » (ou sensibilisation IgE-médiée ») étant préférable. Récemment, certaines firmes ont voulu promouvoir le dosage des IgG (en particulier des IgG4) dirigées contre certains allergènes, en particulier les aliments, comme des « marqueurs » d’une réaction allergique. Cette interprétation est fausse et a bien été confirmée comme telle par les diverses sociétés savantes. En effet, la présence d’IgG contre les aliments (et les autres sortes d’antigènes) est une réaction normale du système immunitaire(1).
Historique
Si, de nos jours, la fréquence des allergies multiples est reconnue, elle ne l’était pas au début des années 1990 où le SAM était un phénomène nouveau, contemporain de « l’explosion de fréquence des allergies », parmi lesquelles les AA, tout particulièrement à l’arachide(2).
• En 1991, Paupe et Scheinmann(3) ont rapporté 40 cas d’enfants qui avaient développé « une dermatite atopique, un asthme et une allergie alimentaire plus ou moins complexe ». La durée d’observation, de 19 mois à 16 ans, était ≥ 5 ans dans 72,5 % des cas. Fait important, la fréquence de cette association, faible chez les enfants nés entre 1973 et 1977, augmentait brusquement à par tir de 1977. La plupart de ces enfants avaient une hyper-IgE, c’est-à-dire une augmentation des IgE sériques totales très largement supérieures aux valeurs normales attendues pour l’âge(a). Pour les auteurs, ces manifestations étaient indépendantes les unes des autres, l’amélioration d’une pathologie (par exemple celle de l’asthme) n’ayant pas d’effet sur l’évolution des autres, ce qui nécessitait une prise en charge élective, respiratoire, cutanée et digestive.
• En 1998, Rancé et Dutau(4) ont repris ce thème, se basant sur 45 patients, 26 garçons et 19 filles, âgés de 3 mois à 9 ans au moment du diagnostic. Des antécédents atopiques familiaux au premier degré étaient observés dans près de 80 % des cas. Les IgE totales étaient le plus souvent très élevées car, si les valeurs extrêmes allaient de 7 à 43 900 UI/ml, leur valeur moyenne était de 1 950 UI/ml. La plupart de ces enfants avaient donc une hyperIgE importante. La majorité avaient présenté une DA au cours des premiers mois de leur vie (93,3 %). Les manifestations initiales évocatrices d’AA étaient les suivantes : urticaire (30,3 % des cas), angio-œdème (26,1 %), asthme (10 %), œdème de Quincke (7,3 %). Les autres symptômes étaient plus rares comme le syndrome d’allergie orale (2,3 %), les symptômes digestifs (2,3 %), le choc anaphylactique (1,5 %). Les allergènes alimentaires en cause étaient l’œuf de poule (36 fois), l’arachide (31 fois), la moutarde (23 fois), le lait de vache (20 fois), le poisson (19 fois), et plusieurs autres aliments variés (54 fois). Le diamètre moyen de l’induration induite par les PT était de 8 mm. La moyenne des IgE totales était de 13,2 UI/ml (extrêmes : 0,75-100 UI/ml). Le test de provocation par voie orale (TPO) permettait de préciser la dose réactogène (en moyenne de 900 mg, mais évidemment variable pour chaque aliment).
À cette époque (où on ne réalisait pas d’induction de tolérance orale [ITO]), aucune amélioration ne fut enregistrée chez les allergiques à l’arachide alors qu’une guérison était observée très souvent pour les allergiques au lait de vache (80 % des cas à un âge moyen de 2 ans et 3 mois), souvent pour les allergiques à l’œuf de poule (52,7 % des cas à un âge moyen de 3 ans et 1 mois), et 2 fois respectivement pour le bœuf et le poisson, une fois pour la moutarde et le soja. La DA n’avait évolué favorablement que dans 42,8 % des cas ; l’asthme était apparu en moyenne à 2 ans et 8 mois, et une rhinite était survenue en moyenne à l’âge de 5 ans. Une sensibilisation aux pneumallergènes a été observée chez 35 enfants (77,7 %)(4).
Ces deux séries ont permis de bien observer le « profil clinique » de ces enfants atteints d’allergies multiples IgE-dépendantes, aux aliments et aux pneumallergènes en particulier polliniques, et de symptômes cliniques survenant dans un laps de temps très court(3,4).
La croissance des enfants atteints d’AA multiples pouvant être compromise du fait des évictions alimentaires, Chong et coll.(5) ont étudié 74 enfants (51 % de garçons), 62 (84 %) atteints d’AA IgEdépendantes, 8 (11 %) d’AA mixtes, IgE et non IgE-dépendantes, et 4 (5 %) ayant des AA non IgE-dépendantes. Le nombre des exclusions alimentaires était d’un aliment (55 %), de 2 aliments (27 %), de 3 ou 4 aliments (8 %) et de 5 aliments ou plus (10 %). Ainsi, dans cette étude, près d’un enfant sur 2 avait deux AA ou davantage ce qui, comme nous le verrons plus loin, posait des problèmes nutritionnels (risque de carences alimentaires).
Ces données sont en accord avec les résultats plus anciens de Gupta et coll.(6) obtenus aux États-Unis :
– sur 38 480 enfants, 8 % avaient une AA ;
– parmi ces 8 %, 30,4 % (soit près du tiers) présentaient plusieurs AA ;
– les aliments en cause étaient l’arachide (25,2 %), le lait de vache (21,1 %), les fruits de mer (17,2 %)(6). Ces résultats varient selon les régions du pays(7).
Explorations allergologiques
Les deux principaux objectifs sont de confirmer les véritables allergies et, de ce fait, d’éviter les évictions abusives(5).
Étude de l’anamnèse
Les enfants multiallergiques ont presque toujours des antécédents atopiques familiaux au premier degré (mère et/ou père). Ils présentent presque toujours des antécédents atopiques personnels, en particulier une DA, souvent sévère. Surtout pour les enfants atteints d’AA multiples (ce qui représente le sujet de cette revue), il faut savoir, par un interrogatoire précis, s’il existe des antécédents typiques d’AA vis-à-vis des divers aliments pour lesquels on aura trouvé des PT et/ou des dosages d’IgEs positifs. Ceci est capital car, par exemple, en cas d’AA à l’arachide il est fréquent de trouver des PT positifs et/ou des IgEs élevées dirigées contre d’autres légumineuses ou divers fruits secs à coque, sans qu’il existe une pertinence clinique (terme qui signifie l’absence de réactions antérieures à ces aliments).
Prick-tests cutanés
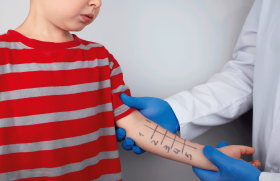
Les prick-tests cutanés d’allergie (PT) sont interprétables dès que la peau est apte à réagir aux témoins positifs, phosphate de codéine à 9 p. 100 (substance entraînant une dégranulation spontanée et non spécifique des mastocytes cutanés) et au chlorhydrate d’histamine à 10 mg/ml (substance qui évalue la réactivité des récepteurs vasculaires H1 à l’histamine)(8). Si ces tests témoins sont positifs (induration d’au moins 3 mm), les PT aux divers allergènes seront interprétables(b). prouvant que la peau présente des mastocytes en quantité suffisante et qu’ils ne sont pas inhibés par un traitement antihistaminique (anti-H1) préalable(c). En pratique, les PT sont réalisables chez 66 % des nourrissons de moins de 1 mois et chez 90 % de ceux de moins de 3 mois. Les PT sont réalisés soit avec des solutions allergéniques commerciales (pneumallergènes, aliments), soit avec des aliments frais (dits natifs), soit pour certains allergènes végétaux avec la pulpe ou en piquant l’allergène végétal (fruit par exemple) puis la peau (technique du « prick plus prick ») (figures 1 à 3).
Figure 1. Réalisation de prick-tests avec des aliments frais. (Coll. G. Dutau)
Figure 2. Même patient : réaction très positive à l’arachide (ARA) à 10-12 mm et encore plus nettement au sésame à 20-22 mm avec pseudopodes et prurit.
Cet enfant se révélera doublement allergique à l’arachide et au sésame. (Coll. G. Dutau)
Figure 3. Lorsque de très nombreux PT doivent être effectués, chez un jeune enfant, la peau du dos peut être utilisée. (Coll. G. Dutau)
Globalement la valeur prédictive négative (VPN)(d) est d’au moins 95 % alors que la valeur prédictive positive (VPP) est inférieure à 50 %. Certains auteurs, dans des circonstances méthodologiques bien précises, ont trouvé une corrélation entre la taille des PT et une forte probabilité de réactivité clinique, mais cette relation manque souvent en pratique. Il faut manier les allergènes avec précaution car, même si les PT sont dépourvus de risque dans la quasi-totalité des cas, il a été décrit des réactions systémiques parfois de type anaphylactique (encadré fin de page, figure 4).
Figure 4. Prick-tests (PT) simultanément positifs à plusieurs poissons. (Coll. G. Dutau)
Il faut cependant se souvenir que ce risque était très important pour les IDR qui ne font plus partie des tests recommandés sauf dans le cas particulier des allergies médicamenteuses.
Dosages des IgE sériques spécifiques
Le dosage des IgE sériques spécifiques (IgEs) offre de nombreux avantages au cours du SAM où l’enfant est souvent atteint de DA étendue et bénéficie de traitements pour ses diverses manifestations allergiques.
En cas d’eczéma, il est admis que les PT peuvent être effectués sur les surfaces de peau non lésée, mais il est peu probable qu’elles soient véritablement « saines » en raison du défaut de la fonction barrière de la peau et du risque de réaction généralisée au cours des PT ne peut être exclu. De toute façon, la présence d’une DA limitera le nombre de PT. Les autres avantages du dosage des IgEs sont nombreux :
– les résultats ne sont pas affectés par les traitements (anti-H1) ;
– leur dosage peut permettre de suivre l’évolution de l’AA (diminution du taux des IgE et augmentation parallèle des IgG4 traduisant l’acquisition d’une tolérance orale [ITO]) ;
– détermination par certaines équipes de valeurs seuils au-dessus desquelles les tests de provocation par voie orale (TPO) ont toute chance d’être positifs ce qui, théoriquement, permettrait de les éviter (?) ;
– par conséquent, existence d’une corrélation entre élévation des IgEs et probabilité d’une réaction clinique. Les inconvénients du dosage des IgEs sont :
– leur coût (limitation des dosages par la nomenclature)(e) ;
– l’absence de corrélation entre le taux des IgEs et la gravité clinique de la réaction ;
– la possibilité de fausses positivités dues à la présence de CDD (pour Cross-reactive Carbihydrate Determinant) pour les allergènes végétaux(f). Par conséquent, pour explorer un SAM il faut habilement combiner les PT et le dosage des IgEs.
Dosage des IgEs dirigées contre les allergènes moléculaires
Depuis une dizaine d’années, le dosage des IgEs dirigées contre des allergènes moléculaires(g), – ou Component Resolved Diagnosis pour Diagnostic par l’analyse des composants allergéniques – naturels et de recombinaison (on dit « allergènes recombinants ») permet de résoudre le diagnostic de situations complexes comme le SAM(9-11).
Parmi de nombreux exemples qu’il n’est tous pas possible d’aborder dans cet article figure l’arachide : sur 4 individus sensibilisés à l’arachide (PT ou dosage d’IgEs positif) un seul est réellement allergique(12). Le dosage des IgEs vis-à-vis des allergènes moléculaires(h) de l’arachide permet de préciser le diagnostic ainsi que la gravité de l’allergie en sachant que le profil de sensibilisation varie selon les pays :
– une AA vraie à l’arachide se traduit par des IgEs contre Ara h 2 (dans la plupart des pays)(in 9) ;
– en Espagne, une AA vraie à l’arachide est associée à des IgEs contre Ara h 9(in 9) ;
– la présence d’IgEs contre Ara h 1, Ara h 2 et Ara h 3 est associée à une AA grave dans plusieurs pays dont la France, le Royaume-Uni)(in 9) ;
– des IgEs contre Ara h 8 sans traduction clinique associées à une allergie au pollen de bouleau sont décrites en Suède(13) et témoignent de réactions croisées.
La découverte des principales familles d’allergènes et leurs sources a permis de faire une avancée décisive dans le diagnostic des AA multiples et pour distinguer les sensibilisations des véritables AA. En substance, il existe des familles biochimiques végétales (albumines 2S, profilines, protéines de transfert lipidique ou LTP [pour Lipid Transfert Protein], etc.) dont les sources appartiennent à des familles botaniques différentes, ce qui explique la possibilité de réactions croisées, soit uniquement biologiques sans pertinence clinique (sensibilisations), soit associées à des symptômes cliniques (allergies vraies) (tableau). Les biopuces, comme l’ImmunoCap ISAC® qui permet, avec une très faible quantité de sérum 30 microlitres (micro - array) de doser les IgEs vis-à-vis de 112 allergènes moléculaires et de 51 sources allergéniques, sont particulièrement adaptées à l’exploration des AA multiples comme :
– l’arachide avec rAra h 1, rAra h 2, rAra h 3, rAra h 8, rAra h 9 et nAra h 6 ;
– la noisette avec rCor a 1, rCor a 8, et nCor a 9 ;
– la noix avec nJug r 1, nJug r 2 et nJug r 3, etc.(i) (9,15).
Ces dosages vont pouvoir estimer la sévérité des AA selon la « formule » (du plus au moins sévère) : « protéines de stockage (PS) > protéines de transport lipidique (LTP) < protéines PR10 (PR10) > profilines (Pr) »(9). Ces dosages ne sont pas remboursés et sont encore du domaine très spécialisé de l’exploration des allergies complexes.
Gestion spécialisée des allergies alimentaires multiples
Induction de tolérance alimentaire
En fonction de ces résultats, les TPO pourront être programmés en cas de responsabilité des PS, des LTP ou des PR10 permettant alors d’affirmer l’AA et de préciser le seuil réactogène de l’allergène alimentaire responsable. Si l’indication d’une induction de tolérance (ITO) est posée (par exemple pour l’arachide), ce qui est du ressort exclusif d’un allergologue entraîné dans la gestion d’une AA, le TPO pourra être répété tous les 6 à 12 mois pour juger de l’évolution de l’AA (et de l’acquisition progressive de la tolérance). La diminution du taux des IgEs (et éventuellement l’augmentation des IgG4 spécifiques). Le lecteur est renvoyé à deux références utiles(16,17) : les principales ITO se font pour l’arachide, le lait de vache, l’œuf de poule, et, occasionnellement pour d’autres aliments (par exemple, le blé, la noisette). En diminuant la dose réactogène, elles permettent de réduire le risque de réaction sévère, et, dans certains cas, d’obtenir une guérison.
Pour l’instant, l’ITO n’est pas indiquée dans les AA multiples ; même si des essais sous anti-IgE ont été effectués(18-20). Le futur de l’immunothérapie aux aliments peut faire appel à d’autres voies comme la voie sublinguale (kiwi, noisette, pêche), à des aliments cuits (lait, œuf), à des traitements additionnels (anti-IgE).
Éducation spécialisée
Un SAM nécessite une éducation précise de l’enfant et de sa famille.
Pour les enfants, les objectifs seront de :
– savoir dénommer une allergie ;
– savoir reconnaître les aliments et refuser les aliments suspects, en particulier à l’école ou hors du domicile ;
– prévenir les adultes en cas d’ingestion douteuse ;
– bien connaître les maniements des médicaments de l’urgence (en particulier celui des stylos auto-injecteurs d’adrénaline).
Pour la famille, les impératifs seront de :
– savoir lire et interpréter les étiquetages ;
– savoir détecter les premiers symptômes d’une allergie alimentaire ;
– savoir que l’adrénaline est le seul traitement de l’anaphylaxie (et connaître sa définition) ;
– savoir utiliser correctement les stylos auto-injecteurs d’adrénaline ;
– demander l’établissement d’un projet d’accueil individualisé en milieu scolaire.
Il faut enfin insister sur le fait que les allergies multiples exposent à un accident allergique aigu grave (AAAG)(18-20). Les phénotypes « multi-sensibilisations » et « multi-morbidités » exposent à des AAAG.
L’adrénaline est le seul traitement de ces accidents dans le cadre d’un plan d’action écrit, régulièrement adapté à l’évolution.
Figure 5. Une unité d’allergologie spécialisé dans la gestion des allergies alimentaires doit avoir une « réserve » d’aliments, régulièrement « mise à jour ». (Coll. G. Dutau)
Références de l'encadré :
1. Novembre E et al. Skin-prick test induced anaphylaxis. Allergy 1995 ; 50(6) : 511-3.
2. Devenney I, Fälth-Magnusson K. Skin prick tests may give generalized allergic reactions in infants. Ann Allergy Asthma Immunol 2000 ; 85(6 Pt 1) ; 457-60.
3. Cantani A, Micera M. Can skin prick tests provoke severe allergic reactions? Eur Rev Med Pharmacol Sci 2000 ; 4(5-6) : 145-8.
4. Liccardi G et al. Anaphylaxis caused by skin prick testing with aeroallergens: case report and evaluation of the risk in Italian allergy services. J Allergy Clin Immunol 2003 ; 111(6) : 1410-2.
5. Liccardi G et al. Systemic reactions from skin testing: litterarure review. J Investig Allergol Clin Immunol 2006 ; 16(2) : 75-8.
6. Codreanu F et al. The risk of systemic reactions to skin prick-tests using food allergens: CICBAA data and literature Review. Eur Ann Allergy Clin Immunol 2006 ; 38(2) : 52-4.
7. Pitsios C et al. Anaphylaxis during skin testing with food allergens in children. Eur J Pediatr 2010 ; 169(5) : 613-5.
8. Galindo-Pacheco LV et al. Anaphylaxis secondary to prick-to-prick tests to foods and its risk factors. Rev Alerg Mex 2014 ; 61(1) : 24-31.
9. Sellaturay P et al. The incidence and features of systemic reactions to skin prick tests. Ann Allergy Asthma Immunol 2015 ; 115(3) : 229- 33.
10. Rancé F et al. Correlations between skin prick tests using commercial extracts and fresh foods, specific IgE, and food challenges. Allergy 1997 ; 52(10) : 1 031-5.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :